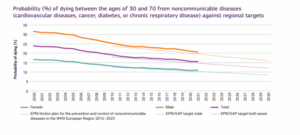
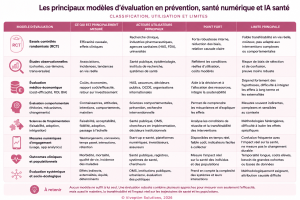
L’OMS vient de publier son rapport sur l’IA en santé « Artificial intelligence is reshaping health systems : state of readiness across the WHO European Region« . L’occasion de s’interroger sur les choix stratégiques d’investissements, alors que les maladies non transmissibles continuent d’exploser, annulant les efforts déjà fournis (Voir notre article sur le sujet).
L’intelligence artificielle, que ce soit en compagnon ou en prédiction / dépistage, est en passe de capter la majeure partie des investissements en santé.
Focus aujourd’hui sur un des domaines d’application encore peu connu, qui contribue au débat : l’avenir de la santé de demain se fera-t-il par l’organisation des soins ou par de nouvelles prises en charge ? Ou un modèle combiné ?
Les modèles d’intelligence artificielle permettent aujourd’hui de prédire avec une précision croissante les admissions hospitalières, les passages aux urgences et la demande de soins. Ces avancées reposent sur des volumes de données sans précédent et des capacités de calcul qui améliorent nettement l’anticipation des besoins.
Ces progrès sont réels. Ils permettent d’optimiser l’allocation des ressources, de mieux gérer les tensions hospitalières et d’améliorer l’organisation des soins.
Mais ils reposent sur une confusion de plus en plus fréquente : améliorer la capacité à anticiper les patients ne signifie pas réduire leur nombre.
Dans un contexte de progression continue des maladies non transmissibles, cette confusion n’est pas neutre. Elle structure les investissements, oriente les priorités et influence les choix stratégiques des systèmes de santé.
En d’autres termes, les systèmes de santé deviennent de plus en plus performants pour gérer des maladies qu’ils ne parviennent pas à réduire.
Des systèmes de santé de plus en plus performants… sur l’aval
Les modèles prédictifs apportent des gains mesurables en matière d’organisation. Ils permettent d’anticiper les pics d’activité, d’ajuster les capacités hospitalières et d’optimiser l’utilisation des lits et des équipes. Dans certains contextes, ils contribuent à réduire les temps d’attente et à améliorer la fluidité des parcours.
Ces bénéfices sont importants, mais ils concernent une partie spécifique du système : la gestion des conséquences.
Autrement dit, ils améliorent la réponse à la demande de soins, sans agir sur les mécanismes qui produisent cette demande.
IA en santé : une réponse efficace… à la mauvaise question
Les modèles prédictifs santé reposent principalement sur des données historiques de soins, des données cliniques et des variables organisationnelles.
Plus une donnée est proche du soin, plus elle est exploitable. Plus elle est proche du comportement, plus elle devient difficile à transformer.
Les modèles prédictifs santé sont conçus pour répondre à une question opérationnelle : combien de patients vont arriver, et à quel moment.
Ils ne répondent pas à une question pourtant centrale pour la santé publique : pourquoi ces patients deviennent-ils patients?
Cette distinction est déterminante. Elle marque la frontière entre une logique d’optimisation du système et une logique de transformation des trajectoires de santé.
Une intervention tardive dans la chaîne de causalité
Dans le continuum de santé, ces modèles interviennent tardivement. Ils se situent après l’exposition aux facteurs de risque, après l’installation des comportements et souvent à proximité immédiate de l’entrée dans le système de soins.
Ils opèrent donc sur des trajectoires déjà largement déterminées.
Plus une cause est en amont, comportementale, environnementale ou sociale, moins elle est captée par les systèmes prédictifs. À l’inverse, plus une situation est proche du recours aux soins, plus elle est modélisable.
Cette asymétrie structure les limites de ces approches.
Mieux gérer sans réduire : une illusion d’efficacité
L’amélioration de la prédiction produit un effet visible : les flux deviennent plus prévisibles, les tensions sont mieux absorbées et le système apparaît plus performant.
Mais dans le même temps, l’incidence des maladies ne diminue pas. Les facteurs de risque persistent et les trajectoires de santé restent inchangées.
Un système peut ainsi devenir très performant dans la gestion des patients tout en traitant un problème qu’il ne réduit pas.
Cette situation crée une illusion d’efficacité : l’amélioration des indicateurs organisationnels masque l’absence de transformation des déterminants de santé.
Le risque systémique : rendre soutenable une trajectoire défavorable
En améliorant la gestion des flux, les systèmes de santé réduisent la visibilité des tensions. Les crises deviennent plus rares ou mieux contrôlées, ce qui renforce l’impression de maîtrise.
Mais cette amélioration peut avoir un effet contre-intuitif : elle rend acceptable un niveau élevé de maladie.
Plus un système est capable d’absorber la demande, moins il est incité à agir sur ses causes. L’optimisation de l’aval peut ainsi contribuer à stabiliser une trajectoire défavorable.
Prédiction et évitement des maladies : deux logiques distinctes
La prédiction et l’évitement des maladies (prise en charge préventive) reposent sur des logiques fondamentalement différentes.
La prédiction vise à optimiser l’existant. Elle améliore l’organisation, l’allocation des ressources et l’efficacité opérationnelle. La prise en charge préventive vise à modifier les trajectoires. Elle agit sur les comportements, les déterminants et, in fine, sur l’incidence des maladies.
Confondre ces deux logiques revient à améliorer le fonctionnement du système sans améliorer la santé de la population.
Pourquoi cette confusion s’installe
Cette confusion s’explique en partie par la compatibilité des modèles prédictifs avec les systèmes existants. Ils s’intègrent facilement dans les infrastructures hospitalières, dans les outils de gestion et dans les logiques de financement.
Ils présentent également un avantage décisif : leurs résultats sont immédiatement mesurables. La réduction des délais ou l’optimisation des ressources sont visibles à court terme, contrairement aux effets de la prise en charge préventive, qui sont diffus, retardés et difficiles à attribuer.
Enfin, ils s’inscrivent dans une logique économique cohérente avec les systèmes actuels, en améliorant l’efficience sans nécessiter de transformation structurelle majeure.
Ce que la réduction des MNT implique réellement
Réduire l’incidence des maladies non transmissibles implique d’agir en amont. Cela suppose de modifier les comportements, de transformer les environnements et de réduire les contraintes qui structurent les choix individuels.
Ces transformations reposent sur des interventions comportementales structurées, des politiques publiques, des mécanismes de régulation et un accompagnement dans la durée.
Ces leviers sont plus complexes à mettre en œuvre, plus coûteux politiquement et moins immédiatement mesurables que l’optimisation des flux de soins.
L’apport et les limites des modèles prédictifs comportementaux
Face à ce constat, il serait logique de tenter d’appliquer des modèles prédictifs à la réduction des risques santé et au changement des comportements santé. Une nouvelle génération de modèles cherche à intégrer les comportements dans la prédiction.
Ces modèles mobilisent des données issues de capteurs, d’applications numériques, d’auto-suivi ou encore des variables contextuelles et psychologiques.
Les résultats récents montrent que l’intégration des données comportementales améliore significativement la capacité de prédiction, sans pour autant améliorer la capacité de transformation.
Des travaux publiés dans npj Digital Medicine en 2023 indiquent que l’intégration de données comportementales améliore la prédiction du risque cardiométabolique par rapport aux seuls indicateurs cliniques.
Des études parues dans Nature Medicine en 2024 montrent que l’utilisation de données longitudinales issues de capteurs permet de détecter plus précocement certaines dégradations de l’état de santé.
Ces résultats confirment que l’intégration du comportement améliore la capacité à prédire.
Mais ils mettent en évidence une limite structurante : prédire un comportement ne signifie pas le modifier.
Ces modèles permettent d’identifier les profils à risque, d’anticiper les ruptures de parcours ou de repérer les moments de vulnérabilité. En revanche, ils n’agissent pas sur les habitudes, les contraintes quotidiennes ou les environnements dans lesquels ces comportements se déploient.
Une revue publiée dans The Lancet Digital Health en 2023 souligne que la majorité des solutions intégrant l’intelligence artificielle restent centrées sur la stratification du risque, la détection et la personnalisation de l’information. Elles interviennent peu sur la modification effective des comportements ou sur les déterminants structurels.
L’intégration des comportements dans les modèles déplace donc la complexité sans la résoudre. Elle permet de mieux comprendre et mieux anticiper, mais pas de transformer.
Conclusion
Les modèles prédictifs, qu’ils soient cliniques ou comportementaux, représentent un progrès important pour l’organisation des systèmes de santé. Ils améliorent la gestion, la planification et la réactivité.
Mais ils ne répondent pas à la question centrale des prochaines décennies : comment réduire le nombre de patients ?
Dans un contexte de progression des maladies non transmissibles, la limite devient structurante. La difficulté n’est plus d’identifier les risques ou de prédire les trajectoires, mais de créer les conditions dans lesquelles ces trajectoires peuvent être modifiées.
Prédire mieux ne suffira pas. La transformation des comportements et des environnements reste le levier décisif. Dans un contexte d’explosion des maladies chroniques, cette distinction n’est plus technique. Elle est stratégique.
Référence
A lire également : 1 cancer sur 2 évitable : à partir de quand une épidémiologie devient-elle réellement reconnue en santé publique ?
aniore, P., Nittas, V., Haag, C., Bernard, J., Gonzenbach, R., & von Wyl, V. (2024). From wearable sensor data to digital biomarker development: Ten lessons learned and a framework proposal. npj Digital Medicine, 7, Article 161. https://doi.org/10.1038/s41746-024-01151-3
Dandan, H., et al. (2025). The comprehensive clinical benefits of digital phenotyping and its role in advancing P4 medicine: A systematic review. npj Digital Medicine. https://doi.org/10.1038/s41746-025-01602-5
Kwon, Y., et al. (2024). Sleep patterns and risk of chronic disease as measured by long-term smartwatch data. Nature Medicine, 30, 2238–2246. https://doi.org/10.1038/s41591-024-03155-8
Maddox, T. M., et al. (2024). Randomised controlled trials evaluating artificial intelligence in clinical practice: A systematic review. The Lancet Digital Health. https://doi.org/10.1016/S2589-7500(24)00047-5
Triantafyllidis, A., Kondylakis, H., Votis, K., Tzovaras, D., & Maglaveras, N. (2023). The global effect of digital health technologies on health workers’ competencies and performance: An umbrella review. The Lancet Digital Health. https://doi.org/10.1016/S2589-7500(23)00092-4
van Spall, H. G. C. (2024). Artificial intelligence bias in the prediction and detection of cardiovascular disease. npj Cardiovascular Health, 1, Article 31. https://doi.org/10.1038/s44325-024-00031-9
Wen, D., et al. (2025). Responsible adoption of multimodal artificial intelligence in health care. The Lancet Digital Health. https://doi.org/10.1016/S2589-7500(25)00099-8
OECD. (2026). The health and economic benefits of tackling non-communicable diseases. OECD Publishing. https://doi.org/10.1787/e20cbbc3-en
World Health Organization. (2025). Noncommunicable diseases. https://www.who.int/news-room/fact-sheets/detail/noncommunicable-diseases